关键词: 教师资格证

扫码添加专属备考顾问
▪ 0元领取考点真题礼包
▪ 获取1对1备考指导
全国教资备考群:737804026(点击进群,群内定期分享教资备考笔面通关资料包,并有客服老师答疑解惑)
内容:
我们知道,物质体积的大小取决于构成这种物质的粒子数目、粒子的大小和粒子之间的距离这三个要素。
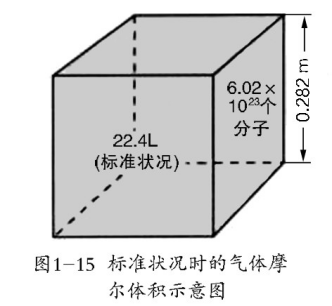
1mol任何物质中的粒子数目都是相同的,即为6.02×1023。因此,在粒子数目相同的情况下,物质体积的大小就主要取决于构成物质的粒子的大小和粒子之间的距离。
1mol不同的固态物质或液态物质含有的粒子数相同,而粒子之间的距离是非常小的,这就使得固态物质或液态物质的体积主要决定于粒子的大小。因为粒子大小是不相同的,所以,1mol不同的固态物质或液态物质的体积是不相同的。
对于气体来说,粒子之间的距离远远大于粒子本身的直径,所以,当粒子数相同时,气体的体积主要决定于气体粒子之间的距离。而在相同的温度和压强下,任何气体粒子之间的距离可以看成是相等的,因此,粒子数相同的任何气体都具有相同的体积。这一规律在19世纪初就已经被发现了。
我们也可以说,在相同的温度和压强下,相同体积的任何气体都含有相同数目的粒子。
单位物质的量的气体所占的体积叫做气体摩尔体积,符号为Vm,常用的单位有L/mol(或L·mol-1)和[m3/mol](或m3·mol-1)
Vm=V/n
气体摩尔体积的数值不是固定不变的,它取决于气体所处的温度和压强。例如,在0℃和101kPa(标准状况)的条件下,气体摩尔体积约为22.4L/mol;在25℃和101kPa的条件下,气体摩尔体积约为24.5L/mol。
基本要求:
(1)要有板书设计;
(2)要有提问互动环节;
(3)试讲中若有实验,实验器具、操作等要进行模拟。
答辩题目:
1. 本节课的教学目标是什么?
2. 气体摩尔体积的大小是不是固定不变的,取决于什么?
试讲答案:
各位考官:大家好,我是高中化学组的XX号考生,我试讲的题目是《气体摩尔体积》,下面开始我的试讲。
一、复习旧知,导入新课
师:我们上节课学习了物质的量,请大家一起回忆我们所学的知识,并回答,什么叫摩尔质量?1摩尔物质的质量是多少?
师:这位同学你来说一下。回答得非常好,没错,单位物质的量的物质所具有的质量就叫做摩尔质量。那么单位物质的量的物质所具有的体积叫什么呢?对,说得非常好,就叫做摩尔体积。怎样理解摩尔体积呢?在相同条件下,1mol不同物质的固体或液体的体积相同吗?1mol不同气体的体积相同吗?我们带着这样的疑问一起来学习今天的内容——气体摩尔体积。
二、新课讲授
师:大家请看PPT,这里有一个表格,请大家一起填写一下,并通过分析表格中,一定温度20℃下,相同物质的量的不同物质的体积的关系,得出固体、液体物质它们的体积有什么规律?
师:大家都填写好了没?哦,都填好了,同学们通过填表,发现了什么规律吗?相同条件下,1mol不同固体或液体物质的体积相同吗?请同学们分小组根据以上表格的信息归纳一下,每组再派代表回答,开始讨论。
师:好,哪组同学先来分享一下你们的讨论结果呢?这位女同学,你们刚才讨论地最热烈,你来说一下吧。
师:哦,你说相同条件下,1mol不同固体或液体物质的体积是不相同的。
师:刚才我们探讨了1mol固体、液体物质的体积,那么,1mol任何气体的体积是否相同呢?请同学们填写PPT上的表格,并思考老师的问题。
师:通过表格我们发现在同温同压时,相同物质的量的不同气体,体积大致相同,那么物质的量都是1mol的不同固体和液体物质,它们的体积各不相同,为什么在同温同压时,同样是1mol的不同气体,体积却大致相同呢?
师:下面老师为大家播放一组投影,通过观察投影,请同学们小组内讨论并总结,从微观粒子角度考虑,决定体积的因素有哪些?开始讨论。
师:好,哪组同学先来说一下你们的看法,好,这位同学,你手举得最高,你来说一下吧。
师:哦,这位同学说,通过第一组“构成固态结构微粒间距离的示意图”、“构成液态结构微粒间距离的示意图”“构成气态结构微粒间距离的示意图”的投影他发现了,液态物质的微粒之间的距离比固态物质的微粒之间的距离大,组成气态物质的微粒之间的距离比它们两者大得多。通过第二组“分子平均距离与分子直径的比较”可以看出固体和液体的体积主要由粒子数目和粒子大小来决定,而气体的体积由于粒子间距远大于粒子直径大小,故主要受分子间的平均距离影响。从而得出,决定物质体积大小的因素有三个:(1)物质的粒子数目,(2)粒子的大小,(3)粒子间的距离。回答得非常好!请坐!
师:通过以上的学习,结合摩尔质量的知识,哪位同学愿意试着从理论上说一下气体摩尔体积的概念?好,这位同学,你来说一下吧。
师:回答得非常好,单位物质的量的气体所占的体积就是气体摩尔体积,请坐!请同学们打开课本看一下气体摩尔体积的概念、符号、公式及常用单位。
三、巩固提高
师:好了,同学们,这就是我们今天学习的重点,下面请同学们做几道习题,巩固一下吧!
师:请大家根据我们这节课所学的知识判断下列说法是否正确?
1. 标准状况下,1mol任何物质的体积大约都是22.4L。
2. 1mol气体的体积约为22.4L。
3. 标准状况下,1molO2和N2混合气体的体积约为22.4L。
4. 22.4L气体所含分子数一定大于11.2L气体所含的分子数。
5. 标准状况下,气体的摩尔体积都是22.4L。
6. 只有在标准状况下,气体的摩尔体积才可能约为22.4L/mol。
四、课堂小结
师:通过刚才的学习我们知道了在相同条件下,1mol固体或液体的体积各不相同,而1mol气体的体积却是几乎相同的。
我们还知道:
1. 决定物质体积大小的因素有三个:(1)物质的粒子数目;(2)粒子的大小;(3)粒子间的距离。
2. 单位物质的量的气体所占的体积叫做气体摩尔体积。
符号为Vm
公式:Vm=

常用单位有L/mol(L·mol-1)和m3/mol(m3·mol-1)。
3. 在标准状况下,1mol任何气体的体积都约是22.4L
师:好,今天的课就上到这里,同学们,下课!
五、板书设计
气体摩尔体积
1. 影响物质体积的三个因素:(1)物质的粒子数目;(2)粒子的大小;(3)粒子间的距离
当微粒个数一定时:固、液体,粒子的大小为主要因素,粒子间的距离为次要因素
气体:粒子间的距离为决定因素
2. 气体摩尔体积
概念:单位物质的量的气体所占的体积
符号:Vm
单位:L/mol
表达式:Vm=

3. 标准状况下的气体摩尔体积(Vm=22.4L/mol)理解要点:
条件:标准状况(S、T、P)
对象:任何气体
物质的量:1mol
我的试讲到此结束,谢谢各位考官的聆听。
答辩答案:
1. (1)知识与技能目标:①能说出气体摩尔体积的概念;②能从宏观和微观两个方面说出影响气体体积的因素;③能进行气体摩尔体积的简单判断和计算。
(2)过程与方法目标:①通过已有知识的迁移理解气体摩尔体积;②通过制作模型和动画演示理解体积的影响因素。
(3)情感、态度与价值观目标:①进一步体会物质的量的“桥梁”作用;②培养分析推理能力,形成良好的学习习惯。
2. 气体摩尔体积的大小并不是固定不变的,取决于温度和压强。在同温同压下,任何气体的气体摩尔体积大小相同。
☟☟☟
添加教师资格客服老师微信
备注“网站”
获取更多考试资讯和海量备考干货


相关推荐:
手机登录确认
微信扫码下载
微信扫一扫,即可下载